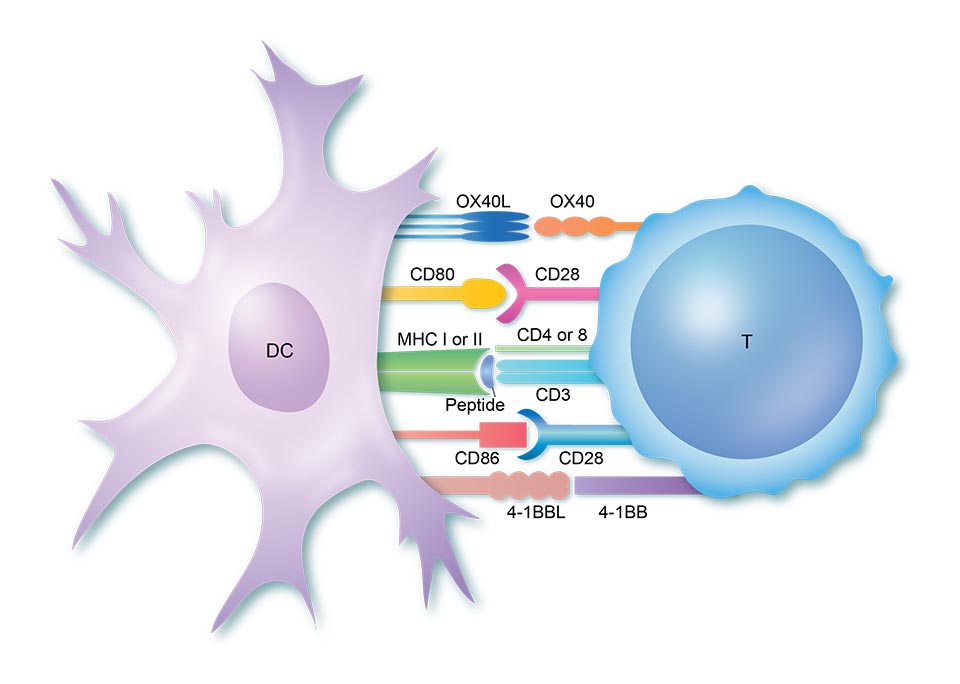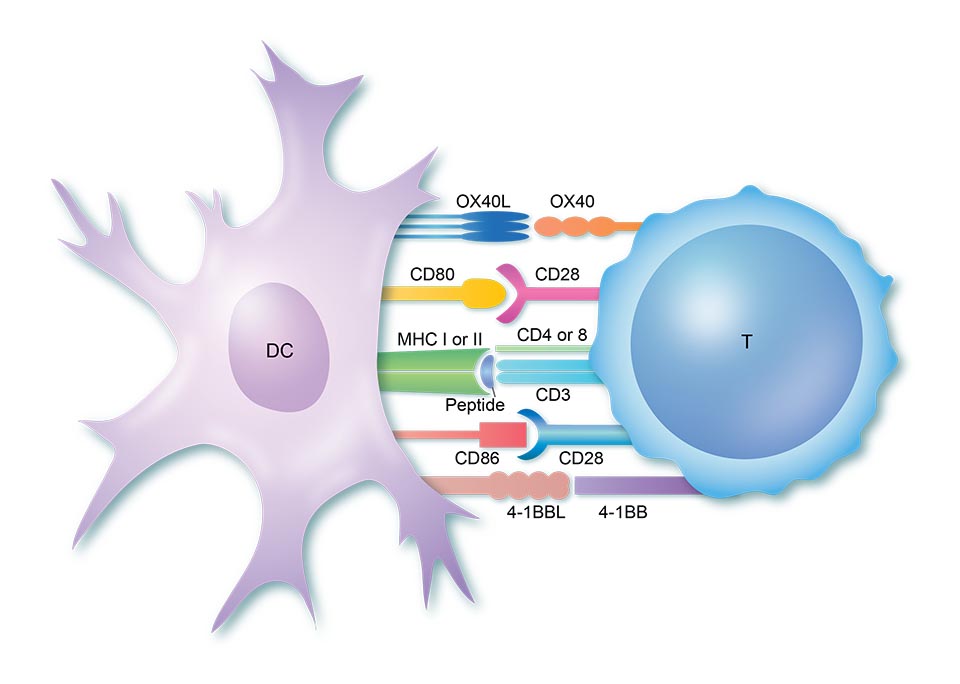
بررسی القای هموگلوبین جنینی (HbF) با ایجاد اختلال در ژن KLF1 با استفاده از فناوری CRISPR در سلولهای بنیادی خونساز انسانی
نیازمندی طرح از لحاظ نیروی انسانی
جهت به انجام رسیدن طرح های عنوان شده به نیروهای متخصص در رشته های ژنتیک، پیوتکنولوژی، ایمونولوژی، نانوتکنولوژی و شیمی نیاز هست.
ویژگیهای اختصاصی داوطلب
دارای مهارت در انجام کشت سلول، جداسازی سلول ها، تمایز سلول ها، دستکاری ژنتیکی، دارای مهارت در انجام تکنیک های مولکولی نظیر استخراج DNA، RNA، پلاسمید، Real-time PCR، PCR، دارای مهارت در انجام تست فلوسایتومتری، مهارت در تولید نانو ذرات